Asam adalah akseptor pasangan elektron. Sebuah contoh berat 05g yang mungkin mengandung NaOH Na 2 CO 3 NaHCO 3 atau campuran NaOH Na 2 CO 3 atau NaHCO 3 Na 2 CO 3 dititrasi dengan 01011M HCL dengan cara dua indicator.
Asam Basa Dan Analisis Kuantitatif Ppt Download
Seperti yang tadi sudah dibahas dari segi rasa asam memiliki rasa yang masam sedangkan basa memiliki rasa yang pahit.

Na2c2o3 asam atau basa. Indikator adalah larutan yang digunakan untuk mengindikasikan secara visual dengan adanya perubahan warna. Asam etilen diamin tetra asetatNCH 2 CH 2 N. TITRASI ASAM - BASA ASIDI ALKALIMETRI lanjutan ASAM-BASA POLIFUNGSIONAL CONTOH.
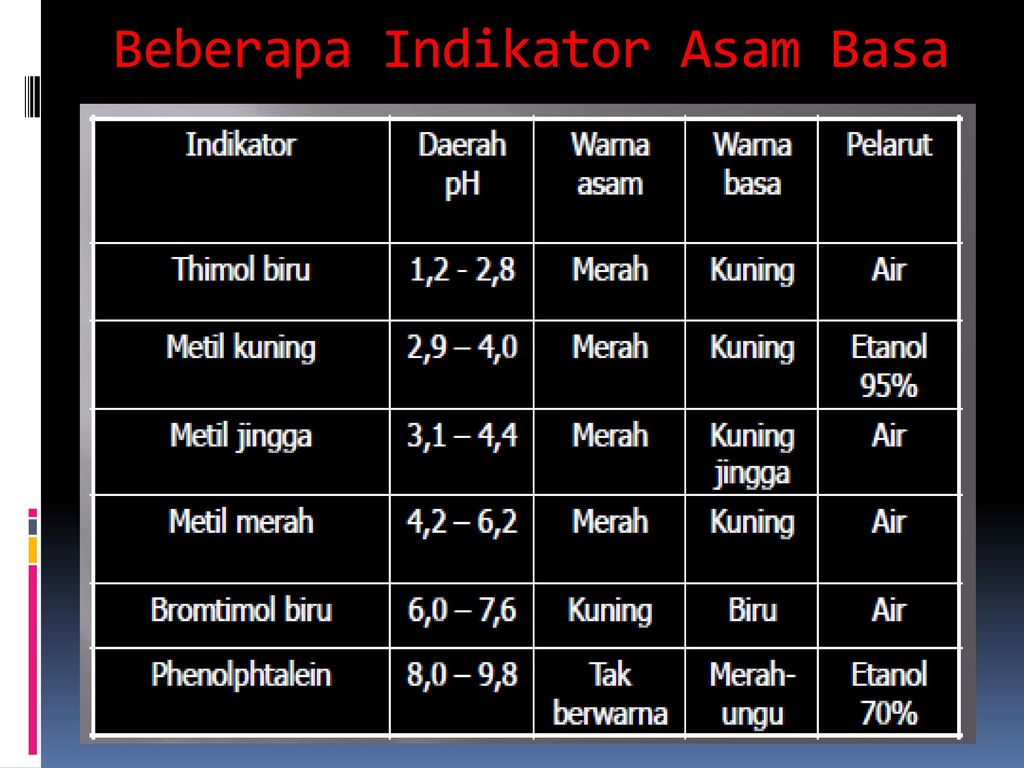
Macam-macam indikator asam basa yaitu Lakmus Metil jingga Metil merah Bromtimol biru dan PP. Sebagai salah satu contoh dari titrasi jenis khusus ini adalah larutan Na2CO3 yang dititrasi dengan larutan HCl. Lalu dari segi pH asam memiliki pH di bawah 7.
HCl H2SO4 HNO3 HClO4 H3PO4 Asam Lemah. Natrium karbonat Na2CO3 Bahan-bahan alat pembersih Natrium hidrogen karbonat NaHCO3 Soda kue Natrium klorida NaCl Garam dapur D. Halo selamat datang di semester 2.
Berikut adalah daftarnya Asam Asam Kuat. NaHCO3 M HCl. Beberapa contoh garam yang dibentuk dari asam kuat dan basa lemah diantaranya adalah Al 2 SO 4 3 AgNO 3 CuSO 4 NH 4 Cl AlCl 3.
Reaksi secara keseluruhan adalah sebagai berikut. Hidroksida atau oksida basa pd pH larutan yg sudah didapar untuk mencegah pengendapan Perlu ditambahkan bahan lain Sophie Damayanti SF. Menghitung pH dari larutan garam yang masih mengandung asam NaHA HA- Contoh.
Ion NH 4 berasal dari basa lemah yaitu NH 3. Suatu larutan berair dari garam semacam itu jelas bersifat basa karena adanya ion OH- tambahan yang dihasilkan oleh hidrolisis anion. Ternyata pada titrasi pertama dengan.
Di tahun 1923 GN. Na2S adalah garam dari asam lemah H2S dan basa kuat NaOH. Contoh basa polifungsional Na2CO3 Reaksi ionisasi dalam dua tahapan.
CuSO4 terbentuk dari basa lemah CuOH2 dan asam kuat H2SO4 Na2CO3 terbentuk dari basa kuat NaOH dan asam lemah H2CO3. Kumpulan pertanyaan tentang asam dan basa berikut pembahasan asam basa. Contohnya adalah Na 2 SO 3 KCN Na 2 CO 3 CH 3 COO 2 Ca.
Contoh Soal Asam Basa Pilihan Ganda dan Jawaban beserta Pembahasan Pada tahun 1923 G. Garam dari basa kuat dan asam lemah garam ini bersifat basa pH 7. Senyawa HClO4 dapat bersifat asam atau basa.
Indikator asam- basa adalah zat yang mengalami perubahan warna dalam larutan. Larutan baku asam dapat dibuat dari HCl H2SO4 atau HClO4 sedangkan larutan baku basa dibuat dari NaOH atau KOH. Di SMP mungkin kalian sudah belajar sedikit mengenai asam basa kali ini kita mau bantu kamu dengan membuat rangkuman materi dan contoh soal asam basa dan titrasi.
Sebagai contoh adalah garam ammonium klorida NH 4 C. Teori Asam Basa Lewis. Bab awal kimia semester 2 untuk kelas 11 adalah asam basa.
Larutan baku primer adalah larutan yang konsentrasinya dapat ditentukan dengan perhitungan langsung dari berat zat yang mempunyai kemurnian tinggi stabil dan bobot ekivalen tinggi kemudian dilarutkan sampai volume tertentu. Basa lemah diprotik atau asam lemah diprotik jika masing-masing kita titrasi dengan asam kuat atau basa kuat maka kita akan memiliki bentuk kurva yang unik. HClO4 NH2- ClO4- NH3.
Garam merupakan suatu senyawa yang terbentuk jika hidrogen Baca Juga Artikel. ASAM EDETAT EDTA H 4 Y Asam Edetat EDTA. Amonium klorida NH 4 Cl terdiri dari kation NH 4 dan anion Cl.
Lewis mengemukakan teori asam basa yang lebih luas dibanding kedua teori sebelumnya dengan menekankan pada pasangan elektron yang berkaitan dengan struktur dan ikatanMenurut definisi asam basa Lewis. Garam dari asam lemah dan basa lemah sifat asambasa bergantung pada nilai Ka dan Kb dari senyawa tersebut. CH3COOH HF HNO2 H2S HCN Basa Basa Kuat.
Jika kamu punya dua larutan tersebut. INDIKATOR ASAM-BASA Untuk mengetahui suatu larutan bersifat asam atau basa salah satunya dapat menggunakan indikator asam basa. Lewis seorang ahli kimia dari Negeri Paman Sam Amerika Serikat memperkenalkan teori asam dan basa.
TITRASI ASAM BASA PENENTUAN KARBONAT BIKARBONAT. Pengertian Larutan Garam Sifat Ciri Jenis dan Contohnya. Reaksi ionisasi dalam tiga tahapan.
April 2 2015 roiyan98 Puisi 7 Komentar. Asam Basa Garam Air Jika HCl dicampurkan dengan NaOH maka ion H dari HCl akan bereaksi dengan ion OH dari NaOH membentuk air H2O. Jadi Na2S juga merupakan garam basa seperti Na2CO3 CaCO3 CH3COONa dll.
Vmj-VppMr NaHCO3 x 100. Apakah Na2S bersifat asam atau basa. Adalah larutan yang didapat dari hasil reaksi asam dan basa.
Sifat larutan garam na2co3. Sifat atau karakteristik asam dan basa dapat kamu lihat pada infografik berikut. Teori ini tidak melibatkan transfer proton melainkan melibatkan penyerahan dan penerimaan pasangan elektron bebas.
Na2CO3 M HClVppMr Na2CO3 x 100. Reaksi yang menunjukkan bahwa HClO4 bersifat asam adalah. Larutan mana sajakah yang termasuk dalam kedalamnya.
M N N CH 2 CH 2 CH 2 O O C O CH 2 C O O CH 2 C O. Oleh bitar Diposting pada 5 Januari 2022. Daftar Asam dan Basa Kuat dan Lemah.
CH 2 COOH CH 2 COOH HOOCCH 2 HOOCCH 2 Sophie Damayanti SF ITB. 73 f 6 Reaksireaksi Asam Basa H2SO4 H2O H3O HSO4 1 HSO4 H2O H3O SO42 2 Ion hidronium yang dihasilkan pada reaksi tahap kedua tidak sebanyak ion hidronium yang dihasilkan pada reaksi tahap pertama. Larutan asam basa memiliki kadar kekuatannya masing-masing dan ada yang termasuk dalam Asam Kuat Asam Lemah Basa Kuat dan Basa Lemah.
Jadi garam uang menghasilkan hidrolisis sempurna yaitu NH42S 3 D Garam. Asam-asam klorida dan sulfat merupakan larutan asam yang paling luas digunakan sebagai larutan standar meskipun tidak satupun mencukupi semua persyaratan di atasGaram klorida dari ion-ion perak timbale dan merkuri I adalah larut seperti halnya sulfat dari logam-logam alkali tanah dan timbaleNamun hal ini tidak menyebabkan kesukaran pada. Berikut daftar Asam Kuat Basa Kuat Asam Lemah dan Basa Lemah-Pada bab asam dan basa SMA IPA Kelas 11 Asam dan basa dibedakan menjadi beberapa golonganAdapun golongan tersebut yakni asam basa kuat serta Asam Basa lemah.
Contoh asam ini antara lain asam sulfat H2SO4 yang dalam air akan berionisasi dalam 2 tahap yaitu. Lewis menyampaikan teori baru mengenai asam basa sehingga partikel ion atau molekul. Standarisasi larutan baku HCL dengan NA2CO3.
Jika 1 mol NaOH 1 mol H2A Reaksi yang terjadi. Contoh ZnNO 2 2 CH 3 COONH 4 Fe 3 PO 4 2. Persamaan reaksinya dapat dituliskan sebagai berikut.
Reaksi penetralan asam kuat dan basa kuat Jika larutan asam dan basa direaksikan maka dihasilkan garam dan air. Dasar Pengelompokan ini tentu ada jika kita tinjau kembali memang keduanya sangat berbeda.

Di Antara Pernyataan Berikut Definisi Asam Menurut Arrhenius Adalah Brainly Co Id